伟德BV1946人工智能微纳传感山西省重点实验室发表题为“基于载谷胱甘肽脂质体分体光电生物传感器原位刺激ATA实现甲胎蛋白高灵敏检测”的研究论文
人工智能微纳传感山西省重点实验室在《Biosensors and Bioelectronics》(SCI一区 IF 10.5)发表题为“基于载谷胱甘肽脂质体的分体式光电化学生物传感器,原位刺激ATA电极实现甲胎蛋白的高灵敏检测” (A split-type photoelectrochemical biosensor using GSH-loaded liposomes in situ stimulation of ATA photoelectrode for the sensitive detection of AFP) 的研究论文。甲胎蛋白(AFP)是肝细胞癌(HCC)与生殖细胞肿瘤的关键临床生物标志物,对其浓度的灵敏与特异检测,在癌症的早期诊断、治疗监测及预后评估中具有重要价值。因此,发展高灵敏度与高特异性的AFP检测方法,对提升临床诊断水平具有重要意义。
光电化学(PEC)是指在光激发下,材料发生电荷分离与转移,从而产生光电流变化的现象。基于PEC的生物传感器因其高选择性、灵敏度和快速响应,在痕量生物分子检测中尤为重要。为提高灵敏度,常引入信号放大策略。其中,脂质体作为载体可将单个生物识别事件转化为多重信号输出,实现高效信号放大。
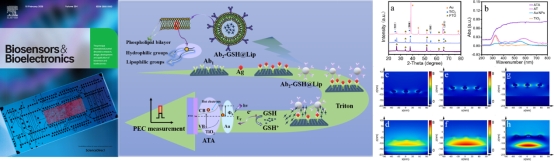
在本工作中,开发了一种基于载谷胱甘肽脂质体(GSH@Lip)的非酶信号放大光电化学(PEC)免疫传感器,用于高灵敏度检测甲胎蛋白(AFP)。该传感器以AuNPs/TiO2/Au(ATA)复合结构为光电极,其独特的光学设计能激发局域表面等离子体共振(LSPR)等多重模式以增强光吸收。经AFP特异性识别与离心富集后,脂质体被裂解释放出大量GSH,后者作为高效电子供体,通过清除空穴有效抑制了ATA电极的电荷复合,从而显著放大光电流信号。此策略无需传统天然酶(如HRP/ALP),稳定性更高、操作更简便。该传感器在10−3至103ng/ml的宽线性范围内表现出优异分析性能,检测下限低至0.86 pg/mL,完全覆盖肝细胞癌(HCC)患者血清AFP的临床相关浓度区间(20–400 ng/mL),为癌症标志物检测提供了一种稳定、灵敏的有效新方法。
课题组博士研究生李敏为本工作第一作者,桑胜波教授、菅傲群教授和薛映仙讲师为通讯作者。本研究得到了国家自然科学基金、山西省重点研发计划的大力支持。

